禾元生物:主攻“稻米造血” 正进行适应症拓展计划 争取2027年实现盈利
禾元生物董事长杨代常说,HY1001作为全球首个植物源重组人血清白蛋白药物,目标是打破我国对进口血浆来源白蛋白的长期依赖,解决国家生物医药领域的供应链安全问题。
新华财经北京12月19日电(记者刘玉龙)今年10月28日,禾元生物在上交所科创板挂牌上市,成为重启未盈利企业适用科创板第五套标准后首家上会企业,也是科创成长层首批新注册企业。上市当天,禾元生物股价以上涨202.82%开盘,随后一周,股票价格曾一度涨至132.02元,较发行价29.06元上涨354.3%,公司市值一度超400亿元。不过,此后伴随市场波动,禾元生物股价有所回调,目前公司市值约260亿元。
新华财经记者调研了解到,虽然相比此前“零产品”未盈利公司上市,禾元生物已有核心产品重组人白蛋白注射液(水稻)(商品名:奥福民)(简称HY1001)取得国家药品监督管理局核准签发的药品注册证书,获批上市,但该产品的商业化及产业化进程存在诸多挑战,相关进展备受投资者关注。
禾元生物董事长杨代常近日接受记者采访时表示,公司已积极通过自建药品销售团队进行学术推广以及发展商业合作伙伴的方式进行产品销售,制定并正在进行HY1001的临床适应症拓展计划,公司当务之急是为获批药品HY1001的规模化生产和市场供应做准备,努力争取于2027年实现盈利。
通过自建药品销售团队+经销合作推进HY1001商业化
禾元生物成立于2006年,是一家主要从事创新药研发的生物医药企业,目前公司收入主要来自药用辅料、科研试剂等非核心产品,尚未实现盈利。
招股书显示,禾元生物近三年连续亏损,2022年至2024年分别亏损1.44亿元、1.87亿元、1.51亿元。截至2024年末,公司累计未弥补亏损8.51亿元。
今年6月18日,证监会及上交所公布了《关于在科创板设置科创成长层 增强制度包容性适应性的意见》等政策细则,在科创板设置科创成长层,并且重启未盈利企业适用科创板第五套标准上市。
时隔一个月,7月18日,禾元生物科创板IPO注册生效,成为IPO新政后首家注册企业。当天,国家药品监督管理局发布了禾元生物申报的重组人白蛋白注射液(水稻)(商品名:奥福民)获批上市的公告。
中信建投证券新股策略首席分析师张玉龙表示,与此前未盈利上市公司“零产品”IPO、募资主要用于产品研发不同,禾元生物目前主要产品已经成熟,IPO募资主要用于产能建设推进产品商业化。这有助于企业科研成果满足中国健康需求,促进产业化发展,实现更好的投资者回报。
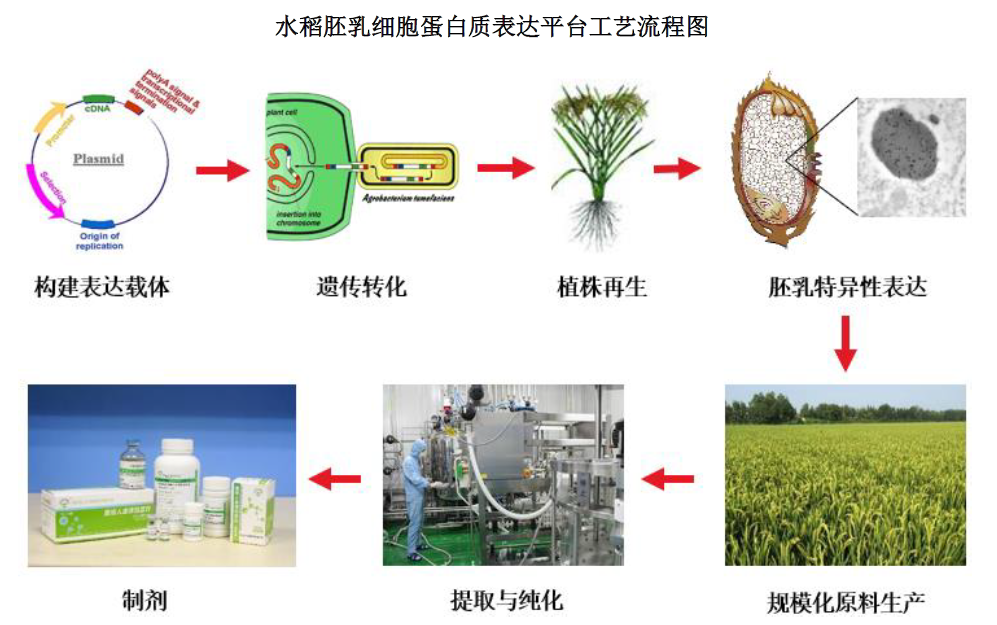
图为水稻胚乳细胞蛋白质表达平台工艺流程图 来源:禾元生物招股说明书
“相较于从人血浆中提取的传统人血清白蛋白,重组人血清白蛋白在生产工艺上具有本质性优势。”倚锋资本CEO朱湃说,它不仅杜绝了血源性疾病传播风险,在批次间一致性、规模化供应保障及生产过程的伦理与环保友好性方面也显著优于传统制备方式,因此具备广阔的市场替代前景。
朱湃表示,目前,该技术路径在国内已实现药品上市的企业仅禾元生物一家,其依托植物(水稻)表达平台生产的重组人血清白蛋白,具有极高的纯度与结构一致性,在安全性与质量可控性上建立了坚实壁垒,形成了显著的先发与技术独占优势。
“我国是全球最大的人血清白蛋白消费市场之一,长期面临供应紧张与安全风险的双重压力。禾元生物的技术突破,为产业提供了稳定、安全、可追溯的替代解决方案。这正是我们在2016至2018年间布局该项目的核心投资逻辑。”朱湃说。
不过,申万宏源证券新股策略首席分析师彭文玉分析,新药品商业化仍需经历市场准入、教育及推广等环节,方能在一定时间后实现成规模的药品销售收入。同时,产品上市后为了保持技术及产品的领先优势,需要持续较大规模的研发投入,公司短期内可能无法实现盈利。
关于HY1001的商业化,杨代常介绍,公司的奥福民®重组人白蛋白注射液(水稻)作为I类创新药,是我国首个批准上市的重组人白蛋白产品。公司已积极通过自建药品销售团队进行学术推广以及发展商业合作伙伴的方式进行产品销售。一方面,公司正在打造一支专业的商业化团队,通过学术营销、临床教育等多种商业化推广方式积极开拓客户资源,打通销售渠道,加快推进核心产品的销售推广工作。另一方面,公司已与国药控股、贝达药业等多家实力雄厚、渠道广布的药品经销商签订经销协议,完成了全国30余个省市区域的销售网络布局。
“我国人血清白蛋白治疗药物市场规模广阔且增长迅速,HY1001已顺利获批上市并按计划逐步放量销售,为公司带来强劲的业绩和充裕的现金流。”杨代常说。
据悉,今年8月,该公司重组人白蛋白注射液(奥福民®)实现首单发运,并于8月23日由医生开出首张处方,首次用于肝硬化低白蛋白血症患者的临床治疗,标志着奥福民®正式进入临床应用阶段。
推进适应症拓展和产业化基地建设
人血清白蛋白,作为人体血浆中含量最丰富的蛋白质,它不仅肩负着维持血浆渗透压、调节体内酸碱平衡的重任,还承担着运输激素、脂类、药物等物质的关键使命,在烧伤、肝硬化、肾病等多种疾病的治疗中不可或缺。
长期以来,人血清白蛋白只能从人血浆中提取,产量有限,我国60%以上依赖进口。禾元生物“稻米造血”,是将人白蛋白基因植入水稻,使水稻在生长过程中合成人白蛋白,并通过提取、纯化等工艺制成注射液。HY1001获批上市,有望在临床上替代血浆来源的人血清白蛋白。
杨代常说,HY1001作为全球首个植物源重组人血清白蛋白药物,目标是打破我国对进口血浆来源白蛋白的长期依赖,解决国家生物医药领域的供应链安全问题。
不过,禾元生物的重组人白蛋白目前仅有一个适应证获批,即用于肝硬化低白蛋白血症(≤30g/L)的治疗。目前,血浆来源白蛋白在临床上可用于治疗因失血、烧伤、烫伤、外科手术引起的循环衰竭、脑损伤等引起的脑水肿、以及肝硬化、肾病综合征等导致的低白蛋白血症等。
因此,HY1001适应症的拓展对其商业化至关重要。
杨代常介绍,公司已制定并正在进行HY1001的临床适应症拓展计划,在进一步与美国食品药品管理局(FDA)沟通具体临床研究方案并达成一致后,将与国家药品监督管理局药品审评中心(CDE)及欧洲药品管理局(EMA)沟通开展一项纳入中国患者、美国患者及欧盟患者的全球多中心III期临床研究,待研究完成后,拟同步向美国FDA及欧洲EMA申报药品上市,并向中国CDE申请HY1001的适应症拓展。预计获批后HY1001将实现在中、美、欧上市销售,并取得血浆来源的人血清白蛋白全部现行适应症。同时,公司正在研究评估在中国拓展适应症的可行性方案。
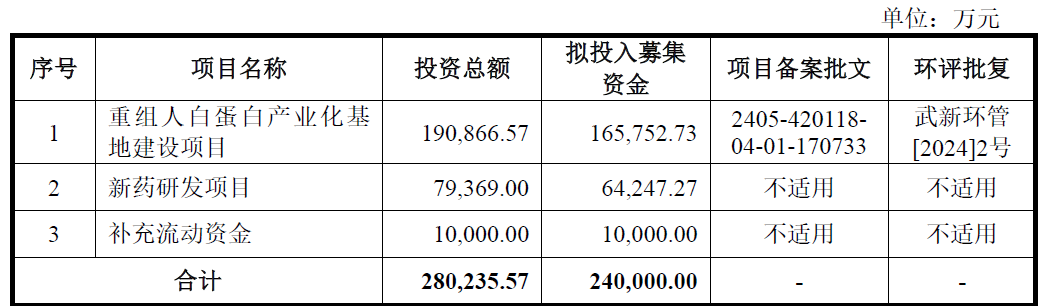
图为禾元生物募资用途情况 来源:禾元生物招股说明书
“上市募资的绝大部分资金投向产业化基地,这与公司的特殊阶段直接相关。”杨代常说,公司当务之急是为获批药品HY1001的规模化生产和市场供应做准备。
杨代常表示,与传统药物生产不同,公司利用“稻米造血”技术,其生产链条延伸至上游农业种植。这需要建设从水稻加工到原液生产的一体化基地。大规模产能本身就是其核心技术(规模化生产能力)的体现和护城河。

图为禾元生物建设中的年产1200万支奥福民的产业化基地 禾元生物供图
他介绍,当前我国人血清白蛋白年需求量巨大,60%以上依赖进口。1200万支/年的设计产能,正是为了快速填补这一战略性的市场空缺。公司120吨重组人白蛋白生产线(年产1200万支)已于2024年9月动工,预计在2026年建成,根据市场需求逐步释放产能。
“公司预计实现规模化生产后,重组人白蛋白注射液的生产成本远低于血浆分离人血清白蛋白的生产成本。”杨代常说,这将有利于提升公司产品竞争力。
杨代常表示,在重点保证HY1001继续研究外,公司将稳步推进其他核心项目的临床试验。同时,公司将加速新靶点、新概念和自身免疫疾病药物等临床未满足领域的新药研发,实现系列产品进入IND(Investigational New Drug)注册。禾元生物以“两新一大”为新药开发策略,即“新靶点新概念大品种”,持续推动新管线研发;同时进一步完善基于重组人白蛋白的长效药物技术平台(OryzDura),推动长效药物进入临床研究。
编辑:罗浩
声明:新华财经(中国金融信息网)为新华社承建的国家金融信息平台。任何情况下,本平台所发布的信息均不构成投资建议。如有问题,请联系客服:400-6123115

















